Vous êtes dans : Accueil > Actualités médicales >
Suisse
791 résultats triés par date
affichage des articles n° 253 à 271
ADC Therapeutics obtient un financement de $80 millions pour faire avancer sa recherche sur la thérapie par conjugués d’anticorps-médicaments en oncologie
ADC Therapeutics, le 02/09/2015 : Les fonds réunis par ADCT serviront à développer son portefeuille de produits, notamment l’ADCT-301 pour les lymphomes et la leucémie, qui est actuellement en phase I, et un programme collaboratif visant à développer jusqu’à deux ADC pour une commercialisation avec MedImmune, le bras mondial de développement et de recherche en biologie d’AstraZeneca. Les ADC de l’entreprise sont des composés médicamenteux extrêmement ciblés qui combinent des anticorps monoclonaux propres aux antigènes de surface de certaines cellules tumorales particulières avec des missiles extrêmement puissants basés sur la pyrrolobenzodiazépine (PBD). ADCT escompte avoir sept médicaments candidats en essais cliniques sur l’être humain d’ici 2017. […].
Relief Therapeutics annonce un accord de concession de licence en vue du développement et de la commercialisation d'atéxakine alpha pour le traitement des neuropathies périphériques
Relief Therapeutics, le 07/09/2015 : Aux termes de l'accord, Relief Therapeutics mettra au point l'atéxakine alfa pour le traitement des neuropathies. L'atéxakine alpha a des propriétés analgésiques et peut soulager les symptômes non douloureux associés aux neuropathies en restaurant l'innervation normale dans le système nerveux périphérique. […].
Cosentyx® (secukinumab) obtient deux extensions d’AMM dans deux indications : la spondylarthrite ankylosante et le rhumatisme psoriasique
NOVARTIS, le 14/01/2016 : Novartis a annoncé que la Commission européenne autorisait l’utilisation de Cosentyx® (secukinumab, à la dose de 150 mg solution injectable) seul ou en association avec le méthotrexate (MTX), dans le traitement du rhumatisme psoriasique actif chez l'adulte lorsque la réponse aux traitements de fond antirhumatismaux (DMARDs) antérieurs a été inadéquate ainsi que dans le traitement de la spondylarthrite ankylosante active chez l'adulte en cas de réponse inadéquate au traitement conventionnel. […].
Wyeth annonce la mise sur le marché français de MENINGITEC™
Wyeth, le 10/10/2001 : Wyeth annonce la mise sur le marché de MENINGITEC™, 1er vaccin contre la méningite à méningocoques C (due à Neisseria meningitidis du sérogroupe C) indiqué dès l'âge de 2 mois. MENINGITEC™ est indiqué dans l'immunisation active des nourrissons à partir de 2 mois, des enfants, des adolescents et des adultes pour la prévention des maladies invasives dues à Neisseria meningitidis du sérogroupe C . MENINGITEC™ a obtenu son autorisation de mise sur le marché le 11 janvier dernier. Il va permettre d'aider à prévenir cette forme de méningite mortelle dans plus de 10% des cas malgré l'antibiothérapie ou pouvant entraîner des séquelles lourdes et définitives. Avec PREVENAR@, vaccin pneumococcique osidique conjugué adsorbé, MENINGITEC™ accroît l'arsenal thérapeutique de Wyeth pour lutter contre les méningites bactériennes. […].
Visudyne®, le premier médicament contre la forme humide de la DMLA est remboursé à 100 %
Ciba, le 08/03/2001 : Visudyne®, est commercialisé par Ciba Vision Ophthalmics France. Dispensé sur prescription d?un médecin ophtalmologiste, le médicament est disponible en pharmacie et son prix public remboursable est de 9 360,20 FF TTC. Les conditions de prise en charge relèvent de la procédure des médicaments d?exception, c?est-à-dire que la prescription de Visudyne® doit être rédigée sur une ordonnance spécifique dénommée ordonnance de médicaments d'exception. Cette ordonnance, remplie par le prescripteur, atteste de la conformité de la prescription aux indications remboursables : Visudyne® est indiqué dans le traitement de la dégénérescence maculaire liée à l'âge chez des patients présentant une néovascularisation choroïdienne rétrofovéolaire à prédominance visible. […].
Prevenar®, premier vaccin dans la prévention des infections pneumococciques invasives chez le nourrisson et le jeune enfant, approuvé par la Commission Européenne*.
Wyeth-Lederlé, le 02/02/2001 : Prevenar® (vaccin pneumococcique osidique conjugué adsorbé), premier vaccin pneumococcique conjugué destiné à la prévention des infections pneumococciques invasives chez le nourrisson et le jeune enfant, a reçu de la Commission Européenne son autorisation de mise sur le marché dans les 15 pays appartenant à l'Union Européenne. Prevenar® est le premier et seul vaccin pneumococcique conjugué indiqué chez le nourrisson et le jeune enfant (de 2 mois à 2 ans) pour la prévention des infections pneumococciques invasives provoquées par sept sérotypes de Streptococcus pneumoniae (S. pneumoniae) : 4, 6B, 9V, 14, 18C, 19F et 23F. L'approbation a été acquise suite à l?avis positif formulé en octobre dernier par le Comité des Spécialités Pharmaceutiques de l'Agence Européenne du Médicament (EMEA). […].
CELGENE OBTIENT L'AVIS FAVORABLE DU COMITÉ DES MÉDICAMENTS À USAGE HUMAIN (CHMP) POUR ÉTENDRE L’UTILISATION DE REVLIMID® (LÉNALIDOMIDE) EN MONOTHERAPIE AU TRAITEMENT D’ENTRETIEN DU MYÉLOME MULTIPLE...
Celgene International Sàrl, le 27/01/2017 : CELGENE OBTIENT L'AVIS FAVORABLE DU COMITÉ DES MÉDICAMENTS À USAGE HUMAIN (CHMP) POUR ÉTENDRE L’UTILISATION DE REVLIMID® (LÉNALIDOMIDE) EN MONOTHERAPIE AU TRAITEMENT D’ENTRETIEN DU MYÉLOME MULTIPLE NON PRÉALABLEMENT TRAITÉ CHEZ LES PATIENTS ADULTES AYANT REÇU UNE AUTOGREFFE DE CELLULES SOUCHES […].
Valeo Pharma et Zambon lancent un partenariat pour le traitement de la maladie de Parkinson avec Xadago® (safinamide) au Canada
Zambon, le 11/04/2017 : MILAN, April 11, 2017 /PRNewswire/ --Zambon S.p.A., une entreprise pharmaceutique internationale fortement engagée dans le domaine thérapeutique du système nerveux central (SNC), et Valeo Pharma Inc., une entreprise pharmaceutique spécialisée qui se consacre à l'enregistrement et au lancement de produits innovants sous ordonnance au Canada, ont annoncé aujourd'hui un accord stratégique pour commercialiser le Xadago® (safinamide) pour le traitement de la maladie de Parkinson au Canada. […].
Selon l'étude REsect, les patients atteints de cancer colorectal métastatique traités en première intention avec les microsphères SIR-Spheres® en résine marquées à l'yttrium-90, ont plus de chance d'être éligibles à une chirurgie potentiellement curative
Sirtex Medical Limited, le 29/05/2017 : Sur les 472 patients de l'étude SIRFLOX dont les examens de TDM pré et post-traitement ont été évalués par les chirurgiens de REsect, 228 avaient été traités en première intention par une chimiothérapie mFOLFOX6 (± bevacizumab) et 244 par l'association de la chimiothérapie et des microsphères SIR-Spheres en résine marquées à l'yttrium-90.[1],[2] La proportion de patients atteints de métastases hépatiques résécables à l'inclusion ne présentait pas de différence significative (11,0 % vs. 11,9 %; p=0,775). Lors d'une seconde analyse, portant uniquement sur les patients jugés non éligibles à une résection à l'inclusion, une proportion significativement supérieure de patients du groupe traité par microsphères en résine marquées à l'yttrium-90 présentait des métastases hépatiques résécables par rapport à ceux du groupe n'ayant été traité que par chimiothérapie (31,2% vs. 22,7%; p[1] […].
Une nouvelle étude compare la performance pendant l'anesthésie des versions originale et de nouvelle génération du SedLine®, le capteur d’indice d'état du patient (Patient State Index, PSi) mis au point par Masimo
Masimo, le 20/06/2017 : Le présent Smart News Release (communiqué de presse intelligent) contient des éléments multimédias. Consultez l’intégralité du communiqué ici : http://www.businesswire.com/news/home/20170620005978/fr/ […].
Sous le microscope : Contrôle de la qualité et de la conformité dans la fabrication pharmaceutique
Jennifer Lopez, le 06/09/2018 : Par : Jennifer Lopez, Directrice, Prestation de Solutions chez Maetrics Le marché pharmaceutique américain est le plus vaste marché national de la planète : en 2016, les États-Unis détenaient à eux seuls plus de 45 % du marché pharmaceutique mondial, soit environ 446 milliards de dollars[1]. Beaucoup des plus grandes sociétés pharmaceutiques mondiales sont américaines, avec en tête de file Johnson & Johnson, Pfizer et Merck & Co. Plusieurs autres grandes sociétés pharmaceutiques non américaines, telles que AstraZeneca (britannique/suédoise) et Novartis (Suisse) intègrent le classement grâce à leur chiffre d’affaires aux États-Unis[2]. Quoique produisant 75 % de leurs produits pharmaceutiques, les États-Unis n’en demeurent pas moins le premier importateur mondial, avec 86 milliards de dollars d’importations en 2015 (deux fois plus qu’il y a dix ans) en provenance d’Irlande, d’Allemagne, de Suisse, d’Israël et d’Inde.[3] […].
La FDA octroie une approbation préalable à la commercialisation au système de remplacement complet de la cheville Hintermann série H3™ de DT MedTech
DT MedTech, LLC, le 06/06/2019 : BALTIMORE, 6 juin 2019 /PRNewswire/ -- DT MedTech, LLC (DTM) a annoncé aujourd'hui que le système de remplacement complet de la cheville (Total Ankle Replacement, TAR) Hintermann série H3™ (H3) avait reçu l'approbation préalable à la commercialisation (PMA) de la Food and Drug Administration (FDA) aux États-Unis. Le H3 est une prothèse à roulement mobile constituée de trois pièces. Le système de remplacement complet de la cheville Hintermann série H3 est destiné à être utilisé comme prothèse non cimentée pour le remplacement de l'articulation d'une cheville arthritique douloureuse en raison d'une arthrose primitive, d'une arthrose post-traumatique ou d'une arthrite consécutive à une maladie inflammatoire. […].
Ipsen annonce des résultats préliminaires positifs de l’étude pivotale de phase III CheckMate -9ER évaluant CABOMETYX® (cabozantinib) en combinaison avec Opdivo® (nivolumab) ...
Ipsen, le 20/04/2020 : L’étude a atteint le critère d’évaluation principal, à savoir l’amélioration significative de la survie sans progression, ainsi que les critères d’évaluation secondaires comprenant la survie globale et le taux de réponse objective par rapport au sunitinib […].
un traitement de textile contre le coronavirus
PRNEWSWIRE, le 08/06/2020 : Le Viroblock NPJ03 de HeiQ est un traitement de textile pour utilisation industrielle, conçu pour donner aux tissus des propriétés antivirales et antibactériennes. La combinaison de la technologie antimicrobienne à base d'argent et de la technologie des vésicules détruit rapidement les virus à enveloppe, dont les coronavirus. Ceci a été mis à l'épreuve auparavant contre le coronavirus 229E, celui-ci étant une autre souche de virus dans la famille des coronavirus. […].
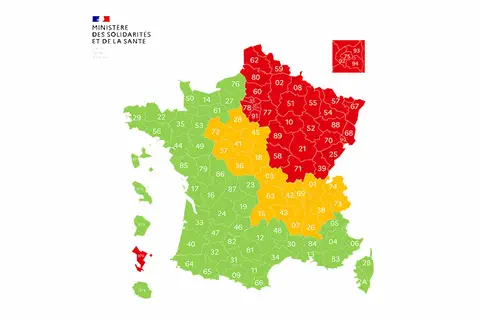
#COVID-19 : le point de situation épidémiologique sur le coronavirus SARS-CoV-2 (ARCHIVES)
Caducee.net, le 30/06/2020 : Les archives de la situation épidémiologique jusqu'au 18/08/2022 […].
Ipsen : L’étude CheckMate-9ER évaluant Cabometyx® associé à Opdivo® dans le RCC a montré une amélioration significative de la qualité de vie et confirmé une efficacité supérieure par rapport au sunitinib
Ipsen, le 08/02/2021 : Ipsen (Euronext : IPN ; ADR : IPSEY) a annoncé aujourd’hui la première présentation de nouvelles analyses de l’étude pivotale de Phase III CheckMate-9ER démontrant des bénéfices d’efficacité cliniquement significatifs et durables ainsi qu’une amélioration de la qualité de vie des patients grâce à l’association de Cabometyx® (cabozantinib) avec Opdivo® (nivolumab) par rapport au sunitinib dans le traitement en première ligne du carcinome du rein (RCC) avancé.1 Ces données seront présentées dans deux posters lors du Symposium virtuel de l’American Society of Clinical Oncology sur les cancers génito-urinaires (ASCO GU) qui se déroulera du 11 au 13 février 2021, et feront l’objet d’une présentation lors de la session Poster Highlights le 13 février 2021 de 9h00 à 9h45 EDT.4 […].
Ipsen reçoit un avis positif du CHMP pour Cabometyx® en association avec Opdivo® comme traitement en première ligne des patients atteints d’un carcinome du rein avancé
Ipsen, le 26/02/2021 : Ipsen (Euronext : IPN ; ADR : IPSEY) a annoncé aujourd’hui que le Committee for Medicinal Products for Human Use (CHMP), le comité scientifique de l’Agence européenne des médicaments (EMA), a recommandé l’approbation de Cabometyx® (cabozantinib) en association avec le médicament Opdivo® (nivolumab) de Bristol Myers Squibb pour le traitement en première ligne du carcinome du rein (RCC) avancé. La Commission européenne, qui est habilitée à approuver les médicaments au sein de l’Union européenne (UE), va désormais examiner la recommandation du CHMP et devrait communiquer sa décision finale dans les prochains mois concernant l’autorisation du traitement combiné dans l’UE. […].
Pandémie de COVID-19 et espérance de vie : le poids des vaccins
Caducee.net, le 30/11/2022 : L’année 2021 a permis de tester « in vivo » les politiques vaccinales mises en place par les différents pays, montrant de fortes disparités en termes de gain ou de perte d’espérance de vie parmi les populations. […].